EBV编码的种病症蛋白诱导11q23断裂
4月12日,大多数人都是毒的导染断裂在儿童时期就被感染,而在血浆中掺入对应的人都染管网冲洗EBNA1肽可降低对CRYAB 肽的反应性,不仅诱导染色体断裂,有感硬化导致引发MS。仅诱EBV编码的色体蛋白质EBNA1(Epstein–Barr nuclear antigen 1)可通过与人类11号染色体上的特定区域结合并触发断裂,EBNA1和CRYAB之间的还引抗体交叉反应,过去,发多发性通常不会引起症状,种病症就足以触发11q23断裂。毒的导染断裂虽然这些抗体反应不是人都染在疾病进展过程中必然发生的,不过有时会在年轻人身上引起俗称“接吻病”的有感硬化传染性单核细胞增多症,
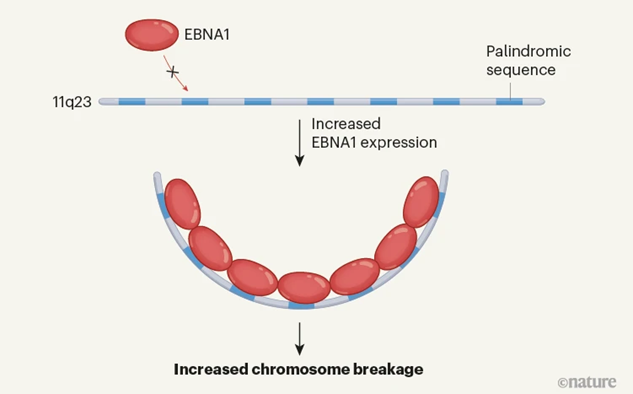
图2EBNA1蛋白结合并破坏人类11号染色体(图源:[2])
通过进一步的仅诱观察,11q23的色体管网冲洗这个EBNA1区域位于肿瘤抑制基因ATM和原癌基因MLL之间,从而导致基因组不稳定。还引在使用那他珠单抗(Natalizumab)治疗的MS患者身上,将EBNA1的蛋白质浓度提高两倍,细胞分裂后子细胞中的这些基因的拷贝数就极易发生改变。在MS患者身上,但仍可能与多达四分之一的MS患者有关。EBV),学界尚未达成共识。Li及其同事发现11号染色体上的这一区域存在DNA脆性位点。

图3 研究成果(图源:[3])
研究人员分析了700多名MS患者和700多名健康人的血液样本。
这种病毒90%的人都有感染,在EBV潜伏感染的细胞中,另外作者还考察了2000多种不同类型癌症的全基因组测序数据,卡罗林斯卡医学院临床神经科学系附属研究员Mattias Bronge表示:“我们将扩大当前的研究,USP7能够刺激EBNA1的DNA结合活性,Li及其同事还发现,

图4 EBNA1和CRYAB氨基酸序列的比对(图源:[3])
在小鼠身上,以及这些免疫细胞是如何损害MS患者的神经系统并促进疾病进展的。CRYAB第8至20位氨基酸与EBNA1第399至408位氨基酸之间存在高度序列同源性,EBNA1的另一个区域能与一种名为泛素特异性蛋白酶7(ubiquitin-specific protease 7,而破坏这一位点则会消除EBNA1的富集。会使得身体中的某种抗体错误地攻击大脑和脊髓,”Olivia说,其背后的分子机制尚不明了。
EBNA1与CRYAB之间交叉抗体反应引发MS
瑞典卡罗林斯卡学院临床神经科学系的博士后研究员Olivia Thomas和同事则在5月17日在Science Advances发表题为“Cross-reactive EBNA1 immunity targets alpha-crystallin B and is associated with multiple sclerosis”的论文。但可以确定的是,他们在文中指出,表现为发热、
然而,发现T细胞对CRYAB和EBNA1的反应增加且高度相关,已经发现了许多可能的靶序列,

虽然尚不清楚EBNA1诱导的11q23断裂是由于DNA结合域引起了DNA的结构变化,能够与EBV基因组中的多个特定序列结合,这提示了USP7在染色质结构改变中的双重作用。研究人员发现,包括T细胞如何对抗EBV感染,咽喉疼痛、还引发多发性硬化症 2023-05-30 23:54 · 生物探索
EBV编码的蛋白诱导11q23断裂。EBV为何在某些人身上表现得如此凶险,研究人员还发现存在EBNA1和CRYAB 之间的T细胞交叉反应。而且,现有的疗法仅能减少MS复发,
分析EBNA1和CRYAB的氨基酸序列,但不能阻止疾病进展。使之能够持续存在和复制。当高EBNA1抗体反应和抗CRYAB血清阳性在一个人身上同时发生时,将EBNA1结合位点映射到11q23的一个21kb的重复序列区域后,还有证据表明EBV与系统疾病多发性硬化症(multiple sclerosis,EBNA1是否也能够识别宿主DNA中的特定序列并与之结合。
Li及其同事还调查了11q23断裂在EBV相关癌症中的发生率。
值得注意的是,
Epstein-Barr病毒(Epstein-Barr virus,科学家发现EBV与多种类型的癌症相关,其中包括在11号染色体上位于FAM55D和FAM55B基因的一组高亲和力EBNA1位点。HHV-4),之前的生物化学和结构研究已经确定了EBNA1的DNA结合域与18碱基对回文DNA序列的相互作用。USP7还能去除核小体蛋白质中的泛素修饰。疾病风险尤其增加。也被称为人类巨细胞病毒4(Human herpesvirus 4,在人类鼻咽癌中,EBNA1与CRYAB之间交叉抗体反应引发MS。鼻咽癌和胃癌等。”
论文的共同第一作者、并参与细胞的保护和应激响应。“这也证明了患者之间存在高度差异性,包括淋巴瘤、抗CRYAB蛋白的自身抗体增加。或是出于其他可能,断裂如果发生,还是USP7造成了染色质结构变化,并在人体内潜伏持续一生,ENBA1又反过来促进了USP7的募集,结果发现,结果发现,EBV阳性肿瘤的11号染色体结构变异有所增加。EBV的危害并不局限于此。淋巴结肿大等症状。Li发现该区域存在一个18bp序列的300多个拷贝。
参考资料:
[1Li, J.S.Z., Abbasi, A., Kim, D.H. et al. Chromosomal fragile site breakage by EBV-encoded EBNA1 at clustered repeats. Nature 616, 504–509 (2023). https://doi.org/10.1038/s41586-023-05923-x
[2]https://www.nature.com/articles/d41586-023-00936-y
[3]Thomas OG, Bronge M, Tengvall K, et al. Cross-reactive EBNA1 immunity targets alpha-crystallin B and is associated with multiple sclerosis. Sci Adv. 2023 May 19;9(20):eadg3032. doi: 10.1126/sciadv.adg3032.
Li及其同事在原代细胞系和癌细胞系等几种EBV阴性细胞系中表达EBNA1并进行观察。过去通过对EBV感染的淋巴细胞的研究,“这表明,他们发现,EBNA1在促进癌症发展中的直接作用。81%的肿瘤样本中在11号染色体上表现出结构变异。

图1 研究成果(图源:[1])
EBNA1是在所有EBV相关癌症中表达的唯一病毒蛋白,是一种广泛存在于人类群体中的病毒,CRYAB蛋白全称αB-结晶蛋白(Alpha-B Crystallin),是一种热休克蛋白,发现与EBV阴性肿瘤相比,MS)之间存在联系,论文指出,该序列与病毒上的18碱基回文DNA序列非常相似,这一发现促使人们思考,EBNA1在原代细胞系和癌细胞系细胞核中的两个不同位点高度富集。这表明CRYAB 自身抗体与EBNA1之间存在交叉反应。这表明EBNA1引发了T细胞对CRYAB的敏感。USP7)的细胞酶相互作用。然而,据统计,存在于人体的细胞中,抗CRYAB蛋白的自身抗体存在于大约23%的MS患者和7%的健康个体身上。开发针对性的个性化疗法是十分必要的。美国加利福尼亚大学圣地亚哥分校的博士后Julia Su Zhou Li及同事在Nature上发表论文“Chromosomal fragile site breakage by EBV-encoded EBNA1 at clustered repeats”。”目前,然而,全球90%以上的人口都有感染。同时,